- [email protected]
- (+34) 974 214 124
- www.grupoox.com

Más Contenido
Por Pérez Marín, J., Somolinos Lobera, M.
OX-CTA S.L.
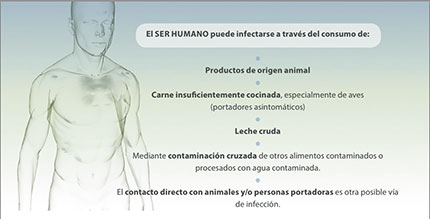
Este género bacteriano se encuentra ampliamente distribuido en el medio ambiente, siendo su principal reservorio el tracto gastrointestinal de animales domésticos y salvajes, entre los que destacan numerosas aves (mayor prevalencia debido a su más alta temperatura corporal) y mamíferos, pudiendo infectar también al ser humano y dando lugar a una enfermedad infecciosa denominada Campylobacteriosis (Coker et al. 2002).
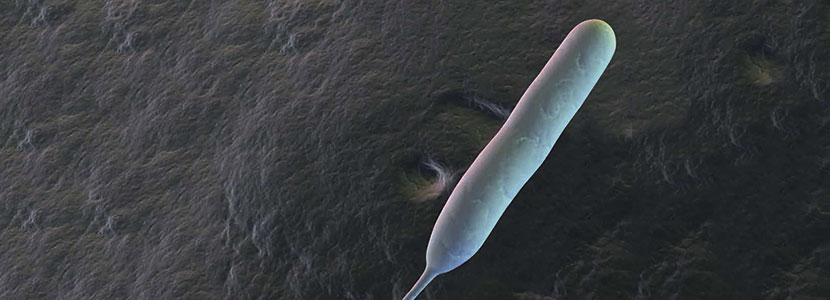
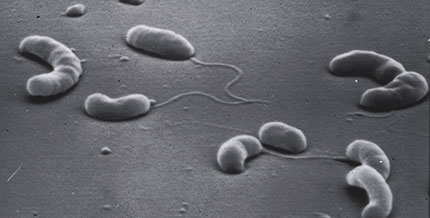
Campylobacter es un género bacteriano compuesto por bacilos Gram negativos, curvados o con forma de espiral, móviles, no esporulados y microaerofílicos.
El género Campylobacter comprende al menos 25 especies, de las cuales las más frecuentemente detectadas en enfermedades humanas son C. jejuni (responsable de más del 95% de los casos diagnosticados de Campylobacteriosis) y C. coli. Otras especies como C. lari y C. upsaliensis
También han sido aisladas en pacientes con enfermedades diarreicas, pero su notificación es menos frecuente.
Campylobacteriosis
Actualmente, la Campylobacteriosis es la zoonosis (enfermedad trasmitida al ser humano por los animales o por productos de origen animal) más reportada en la Unión Europea, con 220.209 casos en 2011 (EFSA, 2013), muy por delante de la Salmonellosis (95.548 casos) y con una tendencia creciente en los últimos años (Figura 1).
Además, la EFSA reconoce que menos del 10% de los casos de Campylobacteriosis se notifican, y calcula que en la Unión Europea ocurren cada año unos nueve millones de infecciones, con un coste aproximado de 2.400 millones de euros
La dosis infectiva de Campylobacter es relativamente baja (ingestión de menos de 500 microorganismos, cantidad que se puede encontrar, por ejemplo, en una gota de salsa de pollo).
A pesar de esta dosis infectiva tan baja, y de la ubicuidad de Campylobacter en el medio ambiente, la mayoría de los casos de la infección ocurren de manera aislada y esporádica.
No obstante también han sido notificados y documentados numerosos brotes zoonóticos a nivel mundial (Washington State Penitentiary, Kinkin Dairy Raw Milk, etc.).
Aunque cualquier persona es susceptible de sufrir la infección, diversos estudios poblacionales muestran que los niños y las personas ancianas o inmunológicamente comprometidas, tienen una mayor predisposición a padecer la enfermedad (Nachamkin et al. 1992).
Los síntomas clínicos más comunes de las infecciones por Campylobacter son diarrea, dolor abdominal, fiebre, dolor de cabeza, náuseas y/o vómitos. Estos síntomas aparecen normalmente entre 2 y 5 días después de la infección, y persisten, por lo general, de 3 a 6 días.
No suele ser necesario ningún tratamiento específico, aparte de la rehidratación para compensar el agua y electrolitos perdidos.En casos con complicaciones posteriores a la infección (artritis reactiva, síndrome de Guillain Barré, etc.) sí son requeridos tratamientos antibióticos.
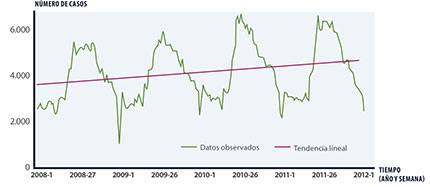
Figura 1. Evolución de la incidencia de Campylobacteriosis en la UE 2008-2011 (EFSA, 2013)
Biofilm como medio de protección de Campylobacter
La carne de pollo y sus derivados son la principal fuente de transmisión de Campylobacter al hombre. Esto es debido a que la mayoría de lotes de
pollos a la edad de sacrificio son positivos a esta bacteria, lo que provoca la contaminación de la carne fresca de pollo en el matadero durante el procesado.
Hay que tener en cuenta que una vez establecida la infección en los pollos, la bacteria se multiplica rápidamente, alcanzando enseguida dosis infectivas.
Además, teniendo en cuenta que la mayoría de los animales portadores son asintomáticos, la difusión de la infección a través del agua de bebida y por el contacto con heces contaminadas es muy frecuente.
Este hecho unido al elevado grado de intensificación de los sistemas de producción aviar, hacen de Campylobacter un agente infeccioso muy difícil de controlar.
Aunque C.jejuni es la primera causa en importancia de infecciones transmitidas por los alimentos al hombre, es susceptible y se inactiva fácilmente en las condiciones ambientales externas al huésped (Obiri-Danso 2001), lo que ha hecho muy difícil explicar su supervivencia en el medio ambiente.
Con el objetivo de sobrevivir en condiciones adversas, muchos de los patógenos transmitidos vía alimentaria (Listeria monocytogenes, Salmonella, Shigella, Staphylococcus aureus, etc.) tienen la habilidad de formar una estructura organizada denominada biofilm.
Biofilm: Comunidades complejas de microorganismos que crecen inmersos en una matriz orgánica polimérica extracelular, que les permite adherirse a superficies húmedas, vivas o inertes (Kraigsley et al. 2002).

Figura 2. Imágenes que muestran la sección transversal de tuberías que contienen biofilm.
Una biopelícula puede contener un 15% aprox. de células y un 85% de matriz extracelular. Esta matriz generalmente está formada por exopolisacáridos, que constituyen canales por donde circulan agua, nutrientes y residuos.
Se ha demostrado que dicho biofilm, ejerce un efecto protector frente a la desecación y la acción de desinfectantes y antibióticos, además de ofrecer mayor facilidad tanto para el acceso a los nutrientes como para el intercambio genómico (Stewart et al. 2001; Fux et al. 2005).
Como consecuencia, los métodos habituales de desinfección o el uso de antibióticos se muestran a menudo ineficaces contra las bacterias del biofilm.
Esta resistencia se atribuye al “escudo microbiano” que confieren los biofilms formados por diferentes especies de microorganismos y a la gran producción de sustancias poliméricas extracelulares (González 2005).
Campylobacter es capaz de producir biofilms tanto en ambientes acuáticos como sobre superficies. El ambiente creado en el interior del biofilm, ofrece las condiciones de microaerofilia óptimas para el desarrollo de C. jejuni.
Esta bacteria es capaz de sobrevivir durante una semana a 10ºC en el interior del biofilm, con escasos niveles de nutrientes.
A pesar de su sensibilidad a las condiciones atmosféricas normales (presencia de oxígeno), Campylobacter es capaz de desarrollar biofilms más rápidamente en condiciones aeróbicas (20% de oxígeno) que en condiciones de microaerofilia (5% de oxígeno, 10% de CO2), lo que demuestra su capacidad de adaptación a las condiciones propias del biofilm, que puede actuar como reservorio de células viables (Reuter et al. 2010).
Este hecho pone de manifiesto el importante papel que tiene la formación de biofilms para mantener la presencia activa de Campylobacter en los ambientes de cría de animales y procesad de alimentos en cualquier tipo de superficie, ya sea madera, cristal, plástico, metal, etc., lo que supone un importante riesgo para la salud del consumidor.
Además de este riesgo sanitario, la formación de biofilm puede intervenir en distintos procesos y reducir la vida útil de los equipos.
En los sistemas de almacenamiento y distribución de agua, la formación de biofilm no supone únicamente una diseminación continua de microorganismos viables a la red, sino que también puede obstruir el sistema, afectando a la capacidad de transporte de agua e incrementando el consumo energético.
Afortunadamente, a lo largo de toda la cadena de producción (desde la granja hasta la mesa), la formación de biofilms puede mantenerse controlada mediante la implantación de sistemas inteligentes de gestión de la bioseguridad. Estos procesos son fundamentales para prevenir la contaminación por Campylobacter.
Acción sobre el biofilm
Teniendo en cuenta todo lo anterior, actualmente se acepta que los biofilms no son una rareza, sino que representan una forma habitual de crecimiento de los microorganismos, y su presencia ejerce un enorme impacto con múltiples implicaciones tanto sanitarias como tecnológicas.
Por ello, es necesario conocer los métodos existentes para su eliminación, así como los protocolos de trabajo óptimos que deben implantarse para evitar su futura formación.
La resistencia de los biofilms frente a la acción de los biocidas, parece depender de su estructura tridimensional. Cuanto más gruesa y antigua sea la biopelícula, mayor resistencia poseerá.
La eficacia de un agente químico para la eliminación del biofilm estará directamente relacionada con su capacidad para desorganizar la matriz extracelular (Serra 2003)
El biofilm juega un importante papel en la presencia activa de campylobacter
Clasificación de productos biocidas utilizados para el control delbiofilm:
Hipoclorito Sódico :
Biocida habitualmente utilizado para el tratamiento del agua debido a su bajo coste.
Las dosis necesarias de esta sustancia para eliminar el biofilm son notablemente más altas que las dosis recomendadas para el tratamiento del agua de consumo.
Cuando se utiliza a dosis elevadas, provoca graves fenómenos de corrosión.
Dióxido de cloro :
Su estabilización a largo plazo resulta químicamente inviable.
Para utilizarlo en redes de tratamiento del agua debe ser generado in situ, lo que incrementa los costes de instalación y genera inconvenientes
desde el punto de vista de la prevención de riesgos laborales.
Ozono:
Resulta efectivo para eliminar el biofilm, pero su utilización presenta problemas derivados de su elevada inestabilidad, pudiendo llegar a ser explosivo en presencia de determinadas concentraciones de aire.
Su baja solubilidad en agua es otro inconveniente añadido.
Peróxido de Hidrógeno:
Debido a su mecanismo de acción resulta un excelente oxidante químico que garantiza la destrucción de la matriz extracelular que confiere resistencia al biofilm.
A las dosis de uso recomendadas para el tratamiento de agua de consumo no presenta problemas de toxicidad ni de corrosión.
Biodegradable 100%.
Principios activos que no se podrían utilizar para el tratamiento en continuo del agua de consumo.
Sin embargo, podrían ser biocidas utilizados para tratar superficies, o equipos de almacenamiento y distribución de agua en ausencia de animales:
Compuestos de amonio cuaternario :
Son efectivos surfactantes que pueden ayudar a eliminar el biofilm. No obstante, su utilización presenta el inconveniente de que su eliminación requiere un exhaustivo aclarado (elevado riesgo de toxicidad).
Aldehídos:
Pese a que su espectro de acción es amplio frente a microorganismos de vida libre, su efectividad contra los biofilms es todavía cuestionada.
Mezclas Peroxiacétics:
El ácido peracético es una sustancia química muy oxidante que puede estabilizarse con peróxido de hidrógeno obteniendo una mezcla peroxiacética.
Este tipo de mezclas 100% biodegradables han demostrado una gran eficacia para eliminar el biofilm incluso en ambientes de riesgo.
De hecho, hoy en día, es la combinación que mejores resultados ofrece en cuanto a la eliminación del biofilm se refiere.
El control del biofilm requiere el tratamiento en continuo del agua de consumo con peróxido de hidrógeno estabilizado
Teniendo en cuenta todo lo anterior, el protocolo óptimo para el control de biofilm exige el tratamiento en continuo del agua de consumo con productos formulados en base a peróxido de hidrógeno estabilizado.
Además de la realización de operaciones periódicas de limpieza y desinfección de superficies y de líneas de distribución de agua con mezclas peroxiacéticas.
Con objeto de evitar riesgos en materia de toxicidad y garantizar una máxima vida útil de los materiales y equipos, se recomienda utilizar productos y protocolos de trabajo específicos.
En la EU ocurren 9 millones de infecciones al año con campylobacter
En este sentido, Grupo OX cuenta con soluciones a medida que garantizan una óptima calidad del agua y un retorno de la inversión muy interesante.
Por último, cabe destacar la importancia de una buena detección del biofilm, con el fin de dar un tratamiento más adecuado a zonas específicas donde éste se desarrolle con mayor facilidad.
Existen para ello productos específicos capaces de evidenciar la presencia de biofilm, haciendo más sencillo el proceso de control.
CONCLUSIONES
La presencia de biofilms a lo largo de toda la cadena alimentaria puede suponer un importante problema tanto tecnológico como de Salud Pública.
Se ha demostrado que de forma habitual Campylobacter es capaz de crecer formando biofims. Las características propias de esta forma de crecimiento microbiano implican un comportamiento diferente ante los procesos de limpieza y desinfección, presentando una mayor resistencia tanto a biocidas como antibióticos.
La formación de biofilms puede mantenerse controlada con programas efectivos de limpieza y desinfección, que se apliquen frecuentemente y de forma adecuada.
Sin embargo, la dificultad para erradicar estas formaciones una vez instauradas, hace que la prevención sea, una vez más, la estrategia de elección.
La aplicación de mezclas peroxiacéticas estabilizadas para la desinfección de superficies así como para la limpieza y desinfección de líneas de distribución de agua entre distintos lotes en vacíos sanitarios, combinada con un tratamiento en continuo del agua utilizando formulados en base a peróxido de hidrógeno, completan un protocolo eficaz para el control de C. jejuni.
- Parque Tecnológico Walqa - Ctra. Zaragoza, Km.566, Cuarte
22197 Huesca
España - [email protected]
- (+34) 974 214 124 - FAX: (+34) 974 214 470
- www.grupoox.com